1. ВВЕДЕНИЕ: ПРИРОДА КОРРОЗИИ В МЕТАЛЛИЧЕСКОЙ УПАКОВКЕ
Коррозия технически определяется как медленное разрушение металла под действием внешнего агента, приводящее к химической или физико-химической атаке. Хотя металлы обычно являются стабильными элементами, вмешательство внешних агентов нарушает это равновесие. В контексте металлической упаковки, в основном из белой жести, это явление имеет решающее значение для целостности продукта и безопасности пищевых продуктов.
Все металлы находятся в контакте с воздухом, состоящим из 79% азота и 21% кислорода. Поскольку азот является инертным газом, агрессивное воздействие атмосферы на металлы почти исключительно приходится на кислород. Однако, чтобы процесс коррозии начался и прогрессировал, кислороду требуются помощники:
- Тепло: Которое вместе с атмосферным кислородом вызывает поверхностное окисление.
- Влажность: Которая в сочетании с кислородом вызывает собственно коррозию.
2. ЭЛЕКТРОХИМИЧЕСКИЕ ОСНОВЫ И ГАЛЬВАНИЧЕСКАЯ ПАРА
Для понимания коррозии в упаковке необходимо понимать электрохимическое поведение металлов. Металлы классифицируются в зависимости от их электрического потенциала:
- Анодные: Металлы с отрицательным потенциалом, которые имеют тенденцию отдавать электроны и легко окисляться.
- Катодные: Металлы с положительным потенциалом (например, благородные металлы), которые притягивают положительные ионы и устойчивы к коррозии.
Когда два разных металла соединяются или вступают в контакт в присутствии электролита, образуется Гальваническая пара. В этой ситуации окисляется металл с более низким потенциалом (самый анодный).
2.1. Конкретный случай белой жести (железо и олово)
Белая жесть демонстрирует увлекательное двойственное поведение в зависимости от того, является ли воздействие внутренним (без кислорода) или внешним (с кислородом).
A) Внутри упаковки (отсутствие кислорода): Олово (Sn) действует как анод по отношению к железу (Fe).
- Реакция: Sn⁰ ⇔ Sn⁺² + 2e⁻ (E₀ = -0,13 В).
- Железо: Fe⁰ ⇔ Fe⁺² + 2e⁻ (E₀ = -0,44 В).
- Олово окисляется, защищая железо. Это явление подразумевает удаление олова, но сохраняет структурную целостность основной стали.
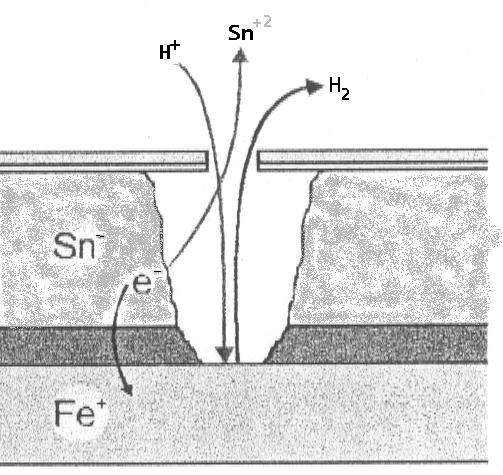
B) Снаружи упаковки (наличие кислорода): Происходит инверсия полярности. Железо ведет себя как анод и окисляется по отношению к олову, которое действует как катод.
- Железо, будучи более электроотрицательным в этой среде, подвергается коррозии.
- Это приводит к образованию оксидов и гидроксидов железа (известной «ржавчины»), цвет которых варьируется от желтого до оранжевого в зависимости от гидратации.
Химические реакции окисления железа следующие: Fe → Fe²⁺ + 2e⁻ (от металла к иону железа) Fe²⁺ → Fe³⁺ + e⁻ (от иона железа к иону железа)
В присутствии влажного воздуха конечным продуктом является гидратированный оксид железа красно-оранжевого цвета: 2 Fe₂O₃ + 6H₂O → 4 Fe(OH)₃
3. КЛАССИФИКАЦИЯ ТИПОВ КОРРОЗИИ
Коррозию можно классифицировать на три основные категории в зависимости от внешнего агента, который ее инициирует.
3.1. Электрохимическая коррозия Это наиболее распространена в металлах, подверженных воздействию влажной атмосферы или погруженных в воду. Она регулируется гальваническими рядами, упомянутыми выше. Классическим примером является поведение железа по отношению к цинку или олову:
- По отношению к цинку (Zn= -0,763 В) железо (Fe= -0,440 В) защищено, потому что цинк более анодный.
- По отношению к олову (Sn= -0,135 В) железо подвергается атаке.
Наличие солей, таких как хлорид натрия (NaCl), ускоряет этот процесс в соответствии с реакцией: 2 ClNa + 2 H₂O ↔ 2 HCl + 2 NaOH Соль реагирует, но не разрушается, способствуя продолжению процесса коррозии до тех пор, пока есть металл и влага.
3.2. Химическая коррозия Вызывается прямым воздействием кислот и щелочей.
- Кислоты: Железо подвергается воздействию неокисляющих кислот. Наличие серы особенно опасно, поскольку образует сульфид железа и действует как катализатор, что делает рискованным использование сернистых соединений в упаковке.
- Щелочи: Атакуют такие металлы, как алюминий и олово. Олово образует растворимые станниты натрия, которые растворяют защитный слой до полного разрушения покрытия.
3.3. Микробиологическая коррозия Это одна из наименее известных, но очень разрушительных форм. Она вызывается действием:
- Анаэробные бактерии: Вырабатывают коррозионные метаболиты.
- Аэробные бактерии: Вырабатывают коррозионные минеральные кислоты.
- Грибы: Производят метаболические органические кислоты.
Метаболизм этих микроорганизмов генерирует газы (CO₂, H₂, N₂) и вещества, такие как аммиак, перекись водорода и сульфиды, создавая высокоагрессивную микросреду для упаковки.
4. РАСПРОСТРАНЕНИЕ И МОРФОЛОГИЯ: ЛОКАЛИЗОВАННАЯ КОРРОЗИЯ
Хотя существует равномерная коррозия (которая поражает всю поверхность), она редко встречается в покрытой упаковке. Наиболее распространенной формой в белой жести является локализованная коррозия, которая поражает определенные области, оставляя другие нетронутыми, обычно из-за дефектов или пористости покрытия (лака или олова).
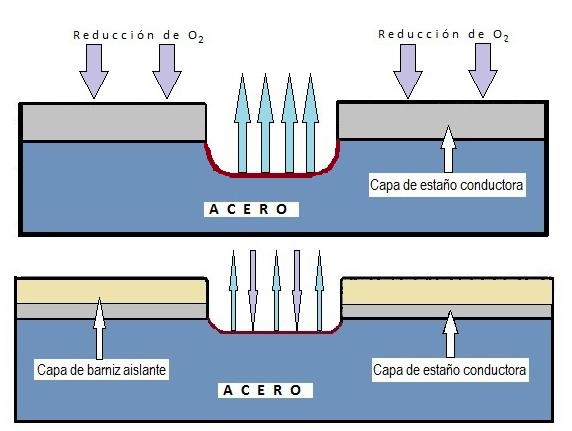
Существует несколько типов локализованной коррозии, имеющих особое значение:
4.1. Межкристаллитная коррозия Поражает соединение зерен в кристаллической структуре металла, ослабляя его механическую прочность и вызывая нерегулярные разрушения. Это не самая распространенная коррозия в упаковке.
4.2. Коррозия в щелях или трещинах (Crevice Corrosion) Возникает в промежутках или скрытых областях, где застаиваются небольшие объемы коррозионных растворов (солей или кислот). Это типично для закрытий упаковки или под кольцами легкого открывания.
4.3. Нитчатая коррозия Это поверхностная вариация, которая происходит под непроводящими покрытиями (лаками). Она характеризуется образованием узких нитей (от 0,05 до 3 мм в ширину), которые извиваются под лаком.
- Механизм: Работает за счет дифференциальной аэрации. «Головка» нити — это анодная зона (где начинается коррозия и происходит закисление), а «хвост» — это наиболее аэрируемая зона.
- Факторы: Требуется относительная влажность выше 60% и наличие солей (хлоридов) в качестве инициаторов.
- Предотвращение: Качество или количество лака не предотвращает его образование; главное — поддерживать низкую влажность и избегать солевых отложений.

4.4. Точечная коррозия (Pitting) Это наиболее распространенная и опасная форма локализованной коррозии. Она возникает в дефектах или плохо аэрируемых зонах (под отложениями). Ее опасность заключается в том, что она проникает в металл вглубь, иногда почти невидимая невооруженным глазом снаружи. Питтинги могут принимать различные морфологии (узкие и глубокие, эллиптические, в галереях и т. д.).
4.5. Коррозия под напряжением (SCC) Подразумевает хрупкое разрушение металла из-за сочетания трех одновременных факторов:
- Растягивающее напряжение (stress).
- Специфическая коррозионная среда.
- Подверженный металл.
Процесс состоит из двух этапов: образование начальной трещины и ее распространение до разрушения материала. Это часто наблюдается в зонах глубокой вытяжки или в заклепках крышек легкого открывания.
4.6. Повреждение водородом Вызвано диффузией водорода в металл, часто ускоряемой сульфидными ионами, происходящими из разложения белков (тиопротеинов) в пище. Основная реакция: 2 H⁺ + 2 e⁻ → H₂↑
5. ФАКТОРЫ ПРОЦЕССА ПРОИЗВОДСТВА И УПАКОВКИ
Внешняя коррозия — это не только проблема материала, но и проблема процесса. Множество этапов влияют на восприимчивость упаковки:
5.1. Механические повреждения и наполнение
- Линии подачи: Трение и удары повреждают внешний лак, обнажая основную сталь.
- Закрытие: Критически важна регулировка закаточных машин. Плохо смазанные ролики или не отрегулированные оправки могут повредить покрытие в зоне закрытия.
- Наполнение: Остатки продукта на упаковке загрязняют воду для стерилизации, повышая ее агрессивность.
5.2. Стерилизация и охлаждение Во время термической обработки в автоклаве:
- Рекомендуется использовать разделители между слоями, чтобы избежать трения в горячем состоянии.
- Воздух, используемый для противодавления, обеспечивает коррозионный кислород.
- Прямое введение пара может увлечь щелочные конденсаты из котлов, которые атакуют лак.
- Сушка: Важно, чтобы конечная температура упаковки позволяла ей «самовысушиваться». Остаточная влага в ковше крышки или под кольцом является питательной средой для гальванических элементов.
6. КАЧЕСТВО ВОДЫ: РЕШАЮЩИЙ ФАКТОР
Технологическая вода (стерилизация и охлаждение) может быть коррозионной или образующей накипь. Ключевые параметры для контроля:
- pH: Кислая или очень щелочная среда атакует металл и лак. Идеальный диапазон: 6,5–8,5.
- Проводимость: Высокие значения (< рекомендуется 2000 мкСм/см) способствуют протеканию тока в гальванических элементах.
- Хлориды и сульфаты: Следует поддерживать на уровне ниже 25 мг/л.
- Сухой остаток (TDS): Менее 500 мг/л.
6.1. Индексы оценки воды Для прогнозирования поведения воды используются специальные индексы:
A) Индекс Ланжелье (LSI): Оценивает равновесие карбоната кальция. Формула: LSI = pH – pHs
- Отрицательный LSI (< -0,4) указывает на коррозионную воду.
- Положительный LSI (> 0,2) указывает на воду, образующую накипь (осаждающую).
B) Индекс Ризнара (RSI): Формула: RSI = 2(pHs) – pH
- Значения >> 7 или 8 указывают на высокую коррозионную активность.
- Значения << 6 указывают на тенденцию к образованию накипи.
Отложения накипи (белые пятна карбонатов) — это не только эстетическая проблема; они действуют как зоны удержания влаги, способствуя последующей коррозии.
6.2. Обработка пассивацией Для смягчения агрессивности воды добавляют катодные ингибиторы (пассиваторы) на основе цинка и фосфорной кислоты. Они создают поверхностное фосфатирование на стали, которое защищает ее. Жизненно важно контролировать дозу, поскольку избыток увеличивает проводимость и, как это ни парадоксально, агрессивность воды.
7. ХРАНЕНИЕ И ТРАНСПОРТИРОВКА: ЭКОЛОГИЧЕСКИЙ КОНТРОЛЬ
После изготовления и обработки упаковка остается в опасности. Внешняя коррозия во время хранения и транспортировки обычно связана с конденсацией и наличием гигроскопичных солей.
7.1. Условия хранения
- Относительная влажность (ОВ): Следует поддерживать на низком уровне (ниже 60%, чтобы избежать нитчатой коррозии).
- Температура: Избегайте резких изменений, которые приводят к точке росы и конденсации.
- Соленость: Солевые отложения притягивают влагу из окружающей среды (гигроскопичность), инициируя коррозию.
- Упаковочные материалы: Картон и разделители не являются инертными; их следует анализировать, чтобы убедиться, что они не содержат агрессивных солей. Использование сплошного пластика может быть контрпродуктивным, если он удерживает внутреннюю влагу.


7.2. Явление конденсации (точка росы) Риск конденсации зависит от соотношения между температурой и относительной влажностью. Если температура внезапно падает, избыток пара конденсируется в жидкую воду на холодных упаковках.
Критические примеры допустимого падения температуры перед конденсацией (для начального воздуха при 35ºC):
- При 20% ОВ: Температура должна упасть на 28ºC (до 7ºC) для конденсации (Низкий риск).
- При 50% ОВ: Достаточно, чтобы она упала на 12ºC (до 23ºC).
- При 75% ОВ: Конденсация происходит при падении всего на 5ºC (до 30ºC) (Очень высокий риск).
Это критично в морских перевозках, где контейнеры подвергаются большим температурным колебаниям.
7.3. Защита от УФ Ультрафиолетовое излучение (солнечное или от люминесцентных ламп в уничтожителях насекомых) разрушает лаки и литографии, ослабляя внешний защитный барьер.
8. МЕТОДЫ ЗАЩИТЫ И ЗАКЛЮЧЕНИЕ
Борьба с коррозией основана на профилактике. Основные стратегии включают:
- Поддержание целостности лака: Поврежденный лак концентрирует анодную атаку.
- Удаление гигроскопичных остатков: Тщательная очистка упаковки после закрытия.
- Абсолютная сушка: Избегайте попадания воды в щели (закрытия, кольца).
- Экологический контроль: Сухие, вентилируемые склады с контролем температуры для предотвращения точки росы.
- Использование ингибиторов: Химическая обработка технологической воды (пассивация).
В заключение, коррозия в металлической упаковке — это многофакторное явление, которое включает в себя химию, металлургию и атмосферную физику, контроль над которым зависит от комплексного управления всем жизненным циклом упаковки.














